Management-Software EU MDRQualitätProjektentwicklungDatenbank
Zu meinen Favoriten hinzufügen
Zum Produktvergleich hinzufügen
Eigenschaften
- Funktion
- Management, Qualität, Projektentwicklung, Datenbank, Sicherheit, Tracking, Supply-Chain, Etikettier
- Anwendung
- Prozess, medizinisch
- Typ
- zentral
- Weitere Eigenschaften
- maßgefertigt
Beschreibung
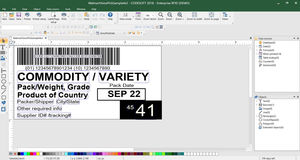
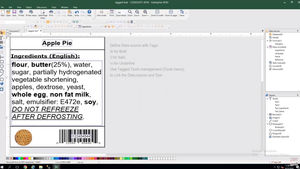
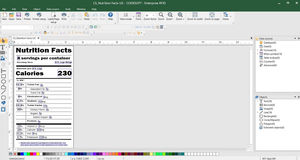
Erstellen und drucken Sie problemlos EU-MDR-konforme Etiketten
CODESOFT für die Erstellung von EU-MDR-Etiketten
Barcode- (HIBC) und GS1 Databar-Barcode-Erstellung für die Gesundheitsbranche
Einfach zu bedienende Assistenten
Erstellen Sie Benutzerrechte und aktivieren Sie die Kontrolle der Etikettensicherheit
TEKLYNX CENTRAL CFR für die Etikettenverwaltung
Ziehen Sie Etikettenelemente aus einer zentralen Datenbank für EU-MDR-konforme Etiketten
Automatisieren Sie den Etikettierungsprozess mit zentraler Verwaltung, um die Durchsetzung des Prozesses und zusätzliche Kontrolle bereitzustellen
Unternehmen, die Medizinprodukte in der gesamten EU vertreiben, müssen die im Mai 2017 festgelegte EU-MDR-Verordnung einhalten.
Die EU-MDR soll die öffentliche Gesundheit und die Patientensicherheit in ganz Europa gewährleisten und die Qualität und Transparenz von Medizinprodukten in der Lieferkette des Gesundheitswesens durch die Gestaltung von Etiketten, die Genehmigung von Etiketten und die Nachverfolgung von Etiketten standardisieren.
Infolgedessen müssen alle Etiketten von Medizinprodukten, mit Ausnahme von Sonderanfertigungen und Produkten für Leistungsstudien/Untersuchungen, einen Unique Device Identifier (UDI) beinhalten, der einen Device Identifier (DI), einen Product Identifier (PI) und Human Readable Information (HRI) umfasst. Hersteller und Vertreiber von Medizinprodukten in ganz Europa müssen die Kennzeichnungsnormen der EU-MDR einhalten.
Die Einhaltung der EU-MDR umfasst:
Der Hersteller muss die UDI-Informationen korrekt an die EUDAMED (Europäische Datenbank für Medizinprodukte) senden und alle UDIs für seine Geräte verwalten
Kataloge
Für dieses Produkt ist kein Katalog verfügbar.
Alle Kataloge von TEKLYNX anzeigenVerwandte Suchbegriffe
- Automatisierungs-Softwarelösung
- Management-Softwarelösung
- Analysesoftwarelösung
- Prozess-Softwarelösung
- Windows-Softwarelösung
- Steuerungssoftwarelösung
- Software für Architektur
- Echtzeit-Softwarelösung
- Online-Software
- Projektentwicklungs-Softwarelösung
- Schnittstellen-Software
- Qualitätssoftware
- Automatisierte Softwarelösung
- Entwicklungssoftware
- Netzwerk-Softwarelösung
- Software für Test
- Entwicklungssoftware
- Reporting-Softwarelösung
- 2D-Software
- Sicherheitssoftware
* Die Preise verstehen sich ohne MwSt., Versandkosten und Zollgebühren. Eventuelle Zusatzkosten für Installation oder Inbetriebnahme sind nicht enthalten. Es handelt sich um unverbindliche Preisangaben, die je nach Land, Kurs der Rohstoffe und Wechselkurs schwanken können.